什么是抗氧化劑?
抗氧化劑可以保護生物系統免受含氧自由基和氧化還原過渡金屬離子(如鐵、銅和鎘)產生的氧化損害[1]。線粒體中的葡萄糖的氧化代謝過程中,超氧陰離子(O2-)作為輔酶Q復合體III還原的副產品產生。超氧化物歧化酶(產品號:S128537)將超氧陰離子轉化為過氧化氫(H2O2),而過氧化氫又可以轉化為過氧自由基(RO2-)、羥自由基(OH-)或次氯酸(ClO-)離子。超氧陰離子還可以與一氧化氮(NO)反應,形成高活性的過氧亞硝基陰離子(ONOO-)[2]。在正常情況下,這些細胞氧化劑被細胞內的抗氧化劑和抗氧化酶還原或清除,其中最重要的是谷胱甘肽(產品號:L274260)、硫氧還蛋白、超氧化物歧化酶、過氧化氫酶(產品號:C163049)和過氧化物酶(產品號:P105528)。飲食中的抗氧化劑,如抗壞血酸(維生素C)、維生素E、β-胡蘿卜素和其他類胡蘿卜素,以及硒,已被認為是細胞和血漿總抗氧化能力的重要成分。類胡蘿卜素、葉黃素和玉米黃素是眼睛和視網膜的重要抗氧化劑[3]。維生素E是生育酚和生育三烯酚的混合物,其中α-生育酚(產品號:T105540)是主要的抗氧化劑[4],是細胞中主要的脂溶性抗氧化劑,在保護膜脂質過氧化方面起著重要作用。低密度脂蛋白(LDL)攜帶維生素E進入細胞,隨后通過向脂肪過氧自由基提供氫氣來防止LDL的過氧化反應[5]。多酚類化合物,特別是黃酮類化合物,最近已被證明是培養細胞中強有力的抗氧化劑。對黃酮類化合物的人體研究也表明,其效果可部分歸因于其抗氧化作用[6]。抗氧化劑可以直接作為還原劑,將質子氫提供給未配對的氧電子,或通過穩定或轉移自由基電子而發揮作用[7]。在這個過程中,還原劑被氧化;例如,兩個谷胱甘肽分子的半胱氨酸巰基被氧化,形成氧化谷胱甘肽的分子間胱氨酸(圖1)。
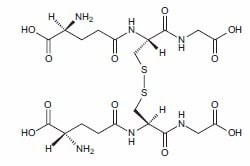
圖1.氧化的谷胱甘肽的結構
膳食抗氧化劑的研究
硫辛酸是一種內源性抗氧化劑,最近作為膳食補充劑受到關注,因為它不僅可以清除自由基,而且它的二氫脂酸鹽形式也是非常有效的還原劑。硫辛酸能減少其他抗氧化劑的氧化形式,并最終能保持組織中還原谷胱甘肽的濃度[8]。一些抗氧化劑捕獲或清除自由基,并在這個過程中成為自由基本身。當類胡蘿卜素蝦青素(圖2)、葉黃素和玉米黃素清除氧自由基時,未配對電子的電荷在分子的整個多烯鏈上變得分散[9]。黃酮醇槲皮素被氧化為醌,可與硫醇反應[10]。 黃酮類化合物也是很好的金屬離子螯合劑,可以防止銅催化的LDL過氧化[1,4,11]。在螯合銅和防止低密度脂蛋白過氧化方面,白藜蘆醇(產品號:R107315)比黃酮類化合物更有效力[12]。這可能有助于白藜蘆醇和黃酮類化合物的抗動脈硬化作用。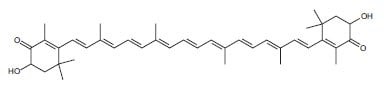
圖2.蝦青素的結構
最新研究進展
Moskaug等人推測,黃酮類化合物通過誘導細胞中的慢性低水平氧化應激來增強細胞的抗氧化系統,從而提高細胞的抗氧化防御系統(激素原理)[15]。 相反,Halliwell等人認為,未被吸收的微摩爾濃度的黃酮類化合物和其他酚類化合物仍然留在小腸和結腸中,它們的抗氧化、金屬螯合和其他作用對結直腸癌的發生有保護作用。最近的研究證實,多酚類物質除了清除自由基和螯合金屬離子外,還具有許多細胞內效應。活性氧(ROS)和活性氮(RNS)也是潛在的信號分子。它們通過一類對氧化還原敏感的轉錄因子調節基因表達的研究,包括誘導抗氧化/解毒酶表達的Nrf2,以及誘導產生炎癥細胞因子、細胞粘附分子、急性期蛋白和抗凋亡的NFkB和AP-1[1,2,16]。這些轉錄因子在應對氧化應激時被激活;持續升高的活性氧(ROS)水平通過誘導其抑制性亞基IkB的磷酸化和分離而激活NFkB。據報道,水飛薊素(產品號:S408123)和水飛薊賓(產品號:S1098009)[17]、兒茶素和原花青素(產品號:P413229),[1,11]以及其他黃酮類化合物[16]可以阻止NFkB的激活。Forman等人引用證據表明,過氧化氫和超氧陰離子通過介導氧化還原信號反應表現出第二信使的特性。他們假設過氧化物與存在于信號蛋白活性部位的關鍵半胱氨酸硫酸鹽可逆地相互作用[18]。已知蛋白酪氨酸磷酸酶和硫氧還蛋白具有硫酸鹽形式的活性部位半胱氨酸,而轉錄因子AP-1和NFkB以及一些半胱天冬酶具有可能是硫酸鹽形式的氧化還原敏感半胱氨酸。一些蛋白激酶c(產品號:P343699)異構體調節部位的鋅結合的半胱氨酸也可能被過氧化氫氧化。受體刺激產生的過氧化物也導致所有有絲分裂原激活蛋白激酶途徑(ERK、JNK和p38 MAPK)的激活。其他信號蛋白和酶是一氧化氮、過氧化物或兩種氧化劑的目標(表1)。因此,清除活性氧中間物的抗氧化劑多酚可能對介導細胞對氧化應激反應的細胞內信號轉導途徑有深遠的影響。
|
信號蛋白
|
調節劑氧化劑
|
|
PTP1B
|
NO, H?O?
|
|
SHP-2
|
H?O?
|
|
LMW-PTP
|
NO, H?O?
|
|
PTEN
|
H?O?
|
|
Trx
|
NO, H?O?
|
|
Src
|
H?O?
|
|
Ras
|
NO, H?O?
|
|
GSTp/JNK
|
H?O?
|
|
Gi/Go
|
H?O?
|
|
NMDA
|
NO
|
表1.氧化還原信號的其他靶點
參考文獻
1. Frei B, Higdon JV. 2003. Antioxidant Activity of Tea Polyphenols In Vivo: Evidence from Animal Studies. The Journal of Nutrition.133(10):3275S-3284S. https://doi.org/10.1093/jn/133.10.3275s
2.Chew BP, Park JS. 2004. Carotenoid Action on the Immune Response. The Journal of Nutrition.134(1):257S-261S. https://doi.org/10.1093/jn/134.1.257s
3.Ribaya-Mercado JD, Blumberg JB. 2004. Lutein and Zeaxanthin and Their Potential Roles in Disease Prevention. Journal of the American College of Nutrition. 23(sup6):567S-587S. https://doi.org/10.1080/07315724.2004.10719427
4.Halliwell B, Rafter J, Jenner A. 2005. Health promotion by flavonoids, tocopherols, tocotrienols, and other phenols: direct or indirect effects? Antioxidant or not?. The American Journal of Clinical Nutrition.81(1):268S-276S. https://doi.org/10.1093/ajcn/81.1.268s
5.Chattopadhyay A, Bandyopadhyay D. 2006. . Vitamin E in the prevention of ischemic heart. . Pharmacological reports . 58(179):179-187. . https://pubmed.ncbi.nlm.nih.gov/16702619/
6.Williamson G, Manach C. 2005. Bioavailability and bioefficacy of polyphenols in humans. II. Review of 93 intervention studies. The American Journal of Clinical Nutrition.81(1):243S-255S. https://doi.org/10.1093/ajcn/81.1.243s
7.Grajek W, Olejnik A, Sip A. Probiotics, prebiotics and antioxidants as functional foods.. Acta Biochim Pol. 52(3):665-671. https://doi.org/10.18388/abp.2005_3428
8.Bilska A, Wlodek L. 2005. . Lipoic acid-the drug of the future. . Pharmacol Rep . 57(5):570-577.. https://pubmed.ncbi.nlm.nih.gov/16227639/
9.Liu RH. 2004. Potential Synergy of Phytochemicals in Cancer Prevention: Mechanism of Action. The Journal of Nutrition.134(12):3479S-3485S. https://doi.org/10.1093/jn/134.12.3479s
10.Moskaug JØ, Carlsen H, Myhrstad MC, Blomhoff R. 2005. Polyphenols and glutathione synthesis regulation. The American Journal of Clinical Nutrition.81(1):277S-283S. https://doi.org/10.1093/ajcn/81.1.277s
11.Keen Cea. 2005. Cocoa antioxidants and cardiovascular health. Am. J. Clin. Nutr.The American Journal of Clinical Nutrition. 81, 298S-303S .https://doi.org/10.1093/ajcn/81.1.298S
12.Pervaiz S. 2003. Resveratrol: from grapevines to mammalian biology.The FASEB journal. 17(14):1975-1985. https://doi.org/10.1096/fj.03-0168rev
13.Crespy V, Williamson G. 2004. A Review of the Health Effects of Green Tea Catechins in In Vivo Animal Models. The Journal of Nutrition.134(12):3431S-3440S. https://doi.org/10.1093/jn/134.12.3431s
14.Schroeter H, Heiss C, Balzer J, Kleinbongard P, Keen CL, Hollenberg NK, Sies H, Kwik-Uribe C, Schmitz HH, Kelm M. 2006. (-)-Epicatechin mediates beneficial effects of flavanol-rich cocoa on vascular function in humans. Proceedings of the National Academy of Sciences. 103(4):1024-1029. https://doi.org/10.1073/pnas.0510168103
15.Scalbert A, Johnson IT, Saltmarsh M. 2005. Polyphenols: antioxidants and beyond. The American Journal of Clinical Nutrition.81(1):215S-217S. https://doi.org/10.1093/ajcn/81.1.215s
16.Surh Y, Kundu JK, Na H, Lee J. 2005. Redox-Sensitive Transcription Factors as Prime Targets for Chemoprevention with Anti-Inflammatory and Antioxidative Phytochemicals.The Journal of Nutrition. 135(12):2993S-3001S. https://doi.org/10.1093/jn/135.12.2993s
17.Kren V, Walterova D. 2005. Silybin and silymarin - new effects and applications. BIOMED PAP. 149(1):29-41. https://doi.org/10.5507/bp.2005.002
18.Forman HJ, Fukuto JM, Torres M. 2004. Redox signaling: thiol chemistry defines which reactive oxygen and nitrogen species can act as second messengers. American Journal of Physiology-Cell Physiology. 287(2):C246-C256. https://doi.org/10.1152/ajpcell.00516.2003